Gas mulia adalah unsur-unsur yang berada di golongan VIIIA. Hal ini sebagaimana selain berfase gas pada suhu ruang, unsur-unsur ini bersifat sangat stabil (sukar bereaksi). Pada awalnya, unsur-unsur ini dikenal dengan istilah gas inert karena tidak ada satupun unsur yang bereaksi dengan unsur lain membentuk senyawa. Barulah pada tahun 1962, Neil Bartlett, seorang ahli kimia asal Kanada, berhasil mensintesis senyawa xenon XePtF6. Sejak saat itu, berbagai senyawa gas mulia berhasil disintesis. Unsur-unsur gas mulia terdiri dari helium (He), neon (Ne), argon (Ar), kripton (Kr), xenon (Xe), dan radon (Rn).
Keberadaan Gas Mulia di Alam
Oleh karena sifatnya yang stabil, di alam gas mulia ditemukan dalam bentuk monoatomik (atom tunggal). Unsur-unsur gas mulia, kecuali radon, dapat ditemukan di udara pada atmosfer meskipun dalam konsentrasi yang sangat kecil. Di antara gas mulia, argon merupakan yang paling banyak terdapat di udara dengan kadar 0,93% dalam udara kering (bebas uap air). Helium lebih banyak ditemukan dalam gas alam (dengan kadar 1%) daripada dalam udara ( 0,00052%). Sementara radon berasal dari peluruhan radioaktif radium dan uranium. Radon juga bersifat radioaktif dan memiliki waktu paro yang relatif pendek sehingga radon akan kembali meluruh menjadi unsur lainnya.
Sifat-sifat Gas Mulia
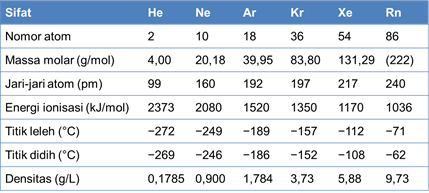
Sifat atomik
Unsur-unsur gas mulia memiliki konfigurasi elektron valensi yang oktet, yaitu ns2 np6, kecuali pada He dengan konfigurasi duplet 1s2. Jari-jari atom dari He ke Rn bertambah sebagaimana bertambahnya jumlah kulit elektron. Konfigurasi elektron dengan kulit valensi terisi penuh demikian menyebabkan gas mulia cenderung sangat stabil (sangat sukar bereaksi).
Selain itu, unsur-unsur gas mulia memiliki energi ionisasi yang sangat besar dan afinitas elektron yang sangat rendah. Energi ionisasi dari He ke Rn semakin berkurang, sebagaimana bertambahnya jari-jari atom sehingga gaya tarik inti terhadap elektron valensi semakin melemah dan energi yang diperlukan untuk melepaskan elektron semakin berkurang.
Sifat fisis
Unsur-unsur gas mulia memiliki titik leleh dan titik didih yang sangat rendah. Titik didihnya hanya beberapa derajat Celcius di atas titik lelehnya. Titik leleh dan titik didih dari He ke Rn bertambah sebagaimana kekuatan gaya London (gaya dispersi) bertambah seiring dengan bertambahnya massa atom dan jari-jari atom.
Densitas (kerapatan) gas mulia juga cenderung bertambah dari He ke Rn. Densitas gas dipengaruhi oleh massa atom, jari-jari atom, dan gaya London. Densitas gas akan bertambah dengan bertambahnya massa atom dan kekuatan gaya London, namun akan berkurang dengan bertambahnya jari-jari atom. Namun demikian, pengaruh massa atom dan gaya London lebih signifikan dibanding pengaruh jari-jari atom dalam hal ini, sehingga densitas bertambah dari He ke Rn.
Sifat kimia
Oleh karena konfigurasi elektron yang stabil, unsur-unsur gas mulia cenderung tidak reaktif (sangat sulit bereaksi). Hal ini didukung oleh fakta bahwa di alam gas mulia selalu ditemukan dalam bentuk monoatomik (atom tunggal). Namun demikian, para ahli telah berhasil mensintesis senyawa gas mulia Ar, Kr, Xe, dan Rn. Kereaktifan unsur meningkat dari Ar ke Rn, di mana dalam reaksi dengan fluorin, Rn dapat bereaksi spontan, Xe memerlukan pemanasan atau penyinaran dengan sinar UV agar reaksi berlangsung, dan Kr hanya bereaksi jika diberi muatan listrik atau sinar X pada suhu yang sangat rendah.
Unsur He dan Ne ditemukan tidak mengalami reaksi kimia dan membentuk senyawa. Unsur Ar diketahui bereaksi dengan HF membentuk senyawa HArF pada suhu 18 K. Unsur Kr dapat bereaksi dengan F2 membentuk senyawa KrF2 dalam kondisi didinginkan pada −196°C dan diberi loncatan muatan listrik atau radiasi sinar X. Unsur Xe dapat bereaksi dengan F2 membentuk tiga senyawa fluorida biner yang berbeda—XeF2, XeF4, dan XeF6—bergantung pada kondisi reaksi dan jumlah reaktan. Unsur Rn bereaksi secara spontan dengan F2 membentuk senyawa RnF2.
Kegunaan Gas Mulia dalam Kehidupan Sehari-hari
Helium
- Helium digunakan sebagai gas pengisi balon udara menggantikan gas hidrogen karena selain ringan juga bersifat inert.
- Helium cair digunakan untuk pendingin koil logam pada alat scanner tubuh (MRI) dan juga pendingin dalam penelitian cryogenics dan superkonduktor sebagaimana titik didihnya yang sangat rendah.
- Helium digunakan sebagai pelarut gas oksigen dalam tabung oksigen penyelam ataupun tabung oksigen rumah sakit. Helium dipilih menggantikan nitrogen karena selain sifatnya inert, kelarutan gas helium dalam darah lebih kecil dibanding gas nitrogen.
Neon
Neon digunakan untuk lampu reklame. Hal ini sebagaimana gas neon dalam tabung bertekanan rendah akan menghasilkan cahaya merah dengan intensitas tinggi jika diberi tegangan listrik.
Argon
- Argon digunakan sebagai gas pengisi dalam beberapa jenis bola lampu karena sifatnya yang tidak reaktif sehingga filamen wolfram tidak mudah putus.
- Argon digunakan sebagai atmosfer inert pada pengelasan; sintesis kristal tunggal silikon atau germanium dalam industri semikonduktor; dan eksperimen dalam glove box di laboratorium.
Kripton
Kripton dapat menghasilkan cahaya putih dengan intensitas tinggi jika diberi muatan listrik sehingga banyak digunakan pada lampu landasan pesawat dan lampu fotografi berkecepatan tinggi.
Xenon
- Xenon digunakan untuk lampu blitz fotografi dan beberapa jenis lampu mobil karena dapat menghasilkan cahaya putih yang sangat terang dengan adanya muatan listrik.
- Xenon dapat digunakan sebagai obat bius (anestetik). Namun, penggunaannya sangat terbatas sehubungan dengan harganya yang sangat mahal.
Radon
- Radon digunakan dalam radioterapi kanker (terapi radiasi) sebagaimana sifatnya yang radioaktif.
- Radon dapat menjadi indikator keberadaan mineral radioaktif seperti bijih uranium dalam tanah, bebatuan, ataupun bahan bangunan.
Contoh Soal Gas Mulia dan Pembahasan
Pernyataan berikut yang bukan merupakan sifat-sifat umum gas mulia, yaitu …
a. terdapat di alam dalam bentuk monoatomik
b. dapat bereaksi spontan membentuk berbagai senyawa
c. titik beku mendekati suhu 0 K
d. sukar melepas dan mengikat elektron
e. kereaktifan unsur semakin meningkat dari atas ke bawah golongan
Jawab:
b. dapat bereaksi spontan membentuk berbagai senyawa
Unsur-unsur gas mulia secara umum cenderung tidak dapat bereaksi spontan membentuk senyawa karena konfigurasi elektronnya yang stabil.
Referensi
Atkins, Peter & Jones, Loretta. 2010. Chemical Principles: The Quest for Insight (5th edition). New York: W.H. Freeman & Company
Brown, Theodore L. et al. 2015. Chemistry: The Central Science (13th edition). New Jersey: Pearson Education, Inc.
House, James E. 2013. Inorganic Chemistry (2nd edition). Oxford: Elsevier
Housecroft, Catherine E. & Sharpe Alan G. 2012. Inorganic Chemistry (4th edition). Harlow: Pearson Education Limited
Johari, J.M.C. & Rachmawati, M. 2008. Kimia SMA dan MA untuk Kelas XII Jilid 3. Jakarta: Esis
McMurry, John E., Fay, Robert C., & Robinson, Jill K. 2016. Chemistry (7th edition). New Jersey: Pearson Education, Inc.
Petrucci, Ralph H. et al. 2017. General Chemistry: Principles and Modern Applications (11th edition). Toronto: Pearson Canada Inc.
Purba, Michael. 2007. Kimia 3A untuk SMA Kelas XII. Jakarta: Erlangga
Retnowati, Priscilla. 2006. SeribuPena Kimia SMA Kelas XII Jilid 3. Jakarta: Erlangga
Shriver, D., et al. 2014. Inorganic Chemistry (6th edition). New York: W.H. Freeman & Company
Artikel: Gas Mulia
Kontributor: Nirwan Susianto, S.Si.
Alumni Kimia FMIPA UI
Materi StudioBelajar.com lainnya:

Leave a Comment