Hidrolisis Garam – Pengantar
Ketika suatu asam bereaksi dengan suatu basa maka akan dihasilkan senyawa ionik yang disebut garam. Larutan garam dapat bersifat netral, asam, ataupun basa. Hal ini dikarenakan terjadinya hidrolisis garam, yaitu reaksi dari suatu kation atau suatu anion, ataupun keduanya, dengan air menghasilkan ion H+(aq) atau OH−(aq).
Secara umum, larutan garam yang dihasilkan dari reaksi asam kuat dengan basa kuat bersifat netral, larutan garam yang dihasilkan dari reaksi asam kuat dengan basa lemah bersifat asam, dan larutan garam yang dihasilkan dari reaksi asam lemah dengan basa kuat bersifat basa.

Garam dari asam kuat dan basa kuat
Garam seperti NaCl yang dapat terbentuk dari reaksi basa kuat (NaOH) dan asam kuat (HCl) tidak dapat terhidrolisis sehingga larutannya bersifat netral. Anion Cl− merupakan basa konjugasi yang sangat lemah karena berasal dari asam kuat sehingga cenderung tidak dapat menarik proton. Kation Na+ tidak terhidrolisis, sebagaimana di dalam air Na+ hanya akan terhidrasi (dikelilingi oleh molekul-molekul H2O). Oleh karena densitas muatannya yang rendah, kemampuan kation Na+ mempolarisasi molekul-molekul H2O di sekitarnya untuk melepas proton dapat diabaikan. Akibatnya, kation Na+ cenderung tidak mempengaruhi keasaman larutan.
- Anion-anion basa konjugasi dari asam kuat yang tidak terhidrolisis, antara lain Cl−, Br−, I−, NO3−, dan ClO4−.
- Kation-kation dari basa kuat yang tidak terhidrolisis, antara lain kation-kation logam golongan IA dan IIA (Li+, Na+, K+, Mg2+, Ca2+), kecuali Be2+.
Jadi, larutan garam dari asam kuat dan basa kuat umumnya tidak mengubah perbandingan konsentrasi H+ dan OH− dalam air. Oleh karena itu, larutannya bersifat netral (pH = 7).
Garam dari asam kuat dan basa lemah
Garam seperti NH4Cl yang dapat terbentuk dari reaksi asam kuat (HCl) dan basa lemah (NH3) akan mengalami hidrolisis kation yang berasal dari basa lemah sehingga larutannya bersifat asam. Anion Cl− tidak terhidrolisis karena merupakan basa konjugasi yang sangat lemah. Kation NH4+ dapat terhidrolisis karena merupakan asam konjugasi lemah yang berasal dari basa lemah sehingga dapat mendonorkan proton (H+) kepada H2O dan membentuk ion hidronium (H3O+).
Kation-kation yang dapat terhidrolisis meliputi:
- kation asam konjugasi dari basa lemah, seperti NH4+, CH3NH3+, C6H5NH3+, dan C5H5NH+;
- kation logam dengan densitas muatan tinggi, seperti Fe3+, Cr3+, Al3+, Cu2+, dan Ni2+.
Jika kation yang terhidrolisis dimisalkan sebagai BH+, maka reaksi hidrolisisnya dapat ditulis sebagai berikut.
BH+(aq) + H2O(l) ⇌ B(aq) + H3O+(aq)
Reaksi ini dapat juga ditulis dalam bentuk yang lebih sederhana seperti berikut.
BH+(aq) ⇌ B(aq) + H+(aq)
![]()
Dengan asumsi jumlah kation BH+ yang terhidrolisis relatif kecil ([BH+]setimbang ≈ [BH+]awal = Mb), sebagaimana kation terhidrolisis merupakan asam konjugasi lemah, maka pada kondisi setimbang: 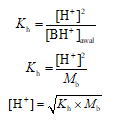
Hubungan antara nilai tetapan kesetimbangan Kh dengan nilai tetapan ionisasi basa lemah B (Kb) dan nilai tetapan autoionisasi air (Kw), yaitu:
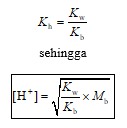
dengan Mb = molaritas komponen kation garam yang terhidrolisis.
Oleh karena itu, larutan garam dari asam kuat dan basa lemah akan meningkatkan konsentrasi H+ (H3O+) dalam air sehingga larutannya bersifat asam (pH < 7).
Garam dari asam lemah dan basa kuat
Garam seperti KCN yang dapat terbentuk dari reaksi asam lemah (HCN) dan basa kuat (KOH) akan mengalami hidrolisis anion yang berasal dari asam lemah sehingga larutannya bersifat basa. Kation K+ tidak terhidrolisis dan juga kation K+ yang terhidrasi memiliki densitas muatan yang rendah sehingga cenderung tidak mempengaruhi keasaman larutan. Anion CN− dapat terhidrolisis karena merupakan basa konjugasi lemah yang berasal dari asam lemah sehingga dapat menarik proton (H+) dari H2O dan membentuk ion hidroksida (OH−).
Anion-anion basa konjugasi dari asam lemah yang dapat terhidrolisis menghasilkan ion OH−, antara lain:
CN−, NO2−, F−, PO43−, CO32−, S2−, HS−, ClO−, C2O42−, HCOO−, CH3COO−, dan C6H5COO−.
Jika anion yang terhidrolisis dimisalkan sebagai A−, maka reaksi hidrolisisnya dapat ditulis sebagai berikut.
A−(aq) + H2O(l) ⇌ HA(aq) + OH−(aq)
![]()
Dengan asumsi jumlah anion A− yang terhidrolisis relatif kecil ([A−]setimbang ≈ [A−]awal = Ma), sebagaimana anion terhidrolisis merupakan basa konjugasi lemah, maka pada kondisi setimbang:
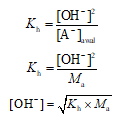
Hubungan antara nilai tetapan kesetimbangan Kh dengan nilai tetapan ionisasi asam lemah HA (Ka) dan nilai tetapan autoionisasi air (Kw), yaitu:
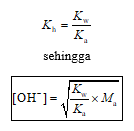
dengan Ma = molaritas komponen anion garam yang terhidrolisis.
Oleh karena itu, larutan garam dari asam lemah dan basa kuat akan meningkatkan konsentrasi OH− dalam air sehingga larutannya bersifat basa (pH > 7).
Garam dari asam lemah dan basa lemah
Garam seperti CH3COONH4 yang dapat terbentuk dari reaksi asam lemah (CH3COOH) dan basa lemah (NH3) akan mengalami hidrolisis kation dan anionnya. pH larutan garam demikian bergantung pada kekuatan asam relatif dari kation dan kekuatan basa relatif dari anion. Kekuatan relatif dari anion dan kation dapat ditentukan dari kekuatan relatif asam lemah dan basa lemah yang berhubungan. Dengan demikian, terdapat tiga kemungkinan kondisi keasaman larutan garam yang terbentuk dengan parameter seperti berikut.

pH larutan garam dari asam lemah dan basa lemah hanya dapat diperkirakan menggunakan rumus berikut dengan asumsi jumlah garam yang terhidrolisis relatif sangat kecil.
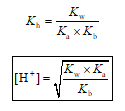
Contoh Soal Hidrolisis Garam dan Pembahasan
Tentukan pH larutan garam berikut dalam air:
a. NaOCl 0,3 M
b. C6H5NH3Cl 0,2 M
c. NH4F 0,1 M
Ka(HOCl) = 2,9 × 10−8; Ka(HF) = 6,6 × 10−4; Kb(C6H5NH2) = 7,4 × 10−10; Kb(NH3) = 1,8 × 10−5
Jawab:
a. Garam NaOCl termasuk garam dari asam lemah (HOCl) dan basa kuat (NaOH), sehingga kation Na+ tidak terhidrolisis sedangkan anion OCl− akan terhidrolisis menghasilkan larutan bersifat basa (pH > 7).
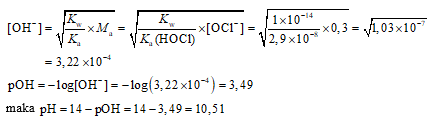
b. Garam C6H5NH3Cl termasuk garam dari asam kuat (HCl) dan basa lemah (C6H5NH2), sehingga anion Cl− tidak terhidrolisis sedangkan kation C6H5NH3+ akan terhidrolisis menghasilkan larutan bersifat asam (pH < 7).
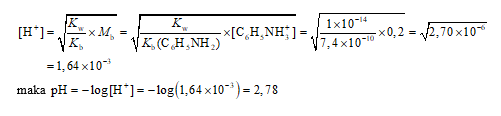
c. Garam NH4F termasuk garam dari asam lemah (HF) dan basa lemah (NH3), sehingga kation NH4+ dan anion F− keduanya terhidrolisis. Oleh karena Ka(HF) (6,6 × 10−4) > Kb(NH3) (1,8 × 10−5), larutan garam akan bersifat asam (pH < 7).
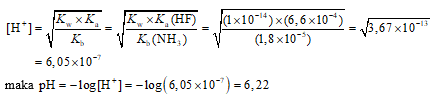
Hidrolisis Garam – Referensi
Atkins, Peter & Jones, Loretta. 2010. Chemical Principles: The Quest for Insight (5th edition). New York: W.H. Freeman & Company
Brown, Theodore L. et al. 2015. Chemistry: The Central Science (13th edition). New Jersey: Pearson Education, Inc.
Chang, Raymond & Goldsby, Kenneth A. 2016. Chemistry (12th edition). New York: McGraw-Hill Education
McMurry, John E., Fay, Robert C., & Robinson, Jill K. 2016. Chemistry (7th edition). New Jersey: Pearson Education, Inc.
Petrucci, Ralph H. et al. 2017. General Chemistry: Principles and Modern Applications (11th edition). Toronto: Pearson Canada Inc.
Purba, Michael. 2006. Kimia 2B untuk SMA Kelas XI. Jakarta: Erlangga
Retnowati, Priscilla. 2005. SeribuPena Kimia SMA Kelas XI Jilid 2. Jakarta: Erlangga
Silberberg, Martin S. & Amateis, Patricia. 2015. Chemistry: The Molecular Nature of Matter and Change (7th edition). New York: McGraw-Hill Education
Artikel: Hidrolisis Garam
Kontributor: Nirwan Susianto, S.Si.
Alumni Kimia FMIPA UI
Materi StudioBelajar.com lainnya:

Leave a Comment