Termokimia adalah ilmu yang mempelajari reaksi kimia dan perubahan energi yang terlibat. Dalam mempelajari termokimia, diperlukan definisi “sistem” dan “lingkungan”. Sistem adalah segala sesuatu yang menjadi fokus perhatian kita. Lingkungan adalah segala sesuatu selain sistem.
Hukum pertama termodinamika menyatakan bahwa energi tidak dapat diciptakan ataupun dimusnahkan. Implikasi hukum ini pada energi dalam sistem, yaitu perubahan energi dalam, ΔE sama dengan penjumlahan kalor (q) yang diserap atau dilepas sistem dengan kerja (w) yang dilakukan atau diterima sistem.
Persamaan Termokimia dan Entalpi
Persamaan termokimia adalah persaman reaksi setara yang menyertakan kalor reaksi (entalpi reaksi) — yang menunjukkan hubungan antara massa dan energi. Contoh persamaan termokimia:
2H2(g) + O2(g) → 2H2O(g) ΔH= −483,6 kJ
Entalpi, H, yaitu fungsi keadaan yang merupakan jumlah dari energi dalam (E) dan hasil kali dari tekanan (P) dan volum (V) sistem. Pada tekanan konstan, perubahan entalpi, ΔH, yang terjadi dalam suatu reaksi disebut juga sebagai entalpi reaksi (ΔHrx) memiliki nilai yang sama dengan kalor reaksi (q).
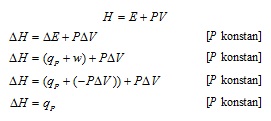
Entalpi reaksi (ΔHrx) juga merupakan fungsi keadaan, yang nilainya bergantung pada Hakhir dan Hawal. Dalam suatu reaksi kimia, “akhir” dan “awal” bisa dinyatakan sebagai “produk” dan “reaktan”. Jadi, Hproduk dapat lebih dari ataupun kurang dari Hreaktan sehingga tanda nilai ΔHrx bergantung pada apakah kalor diserap atau dilepas oleh sistem reaksi. Reaksi disebut eksoterm bilamana melepas kalor sehingga entalpi sistem menurun dan ΔHrx< 0. Reaksi disebut endoterm bilamana menyerap kalor sehingga entalpi sistem meningkat dan ΔHrx> 0.
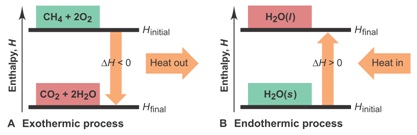
Diagram termokimia: entalpi untuk reaksi eksoterm (A) dan endoterm (B)
(Sumber: Silberberg, Martin S. 2009. Chemistry: The Molecular Nature of Matter and Change (5th edition). New York: McGraw Hill)
Kalorimetri
Kalorimetri adalah cara penentuan kalor reaksi dengan kalorimeter. Kalorimeter merupakan sistem terisolasi (tidak ada perpindahan materi dan energi dengan lingkungan). Jika dianggap keseluruhan kalorimeter adalah sistem, maka qsistem = 0. Dengan mengukur perubahan temperatur (ΔT), dapat dihitung jumlah kalor (q) yang terlibat dalam reaksi di dalam kalorimeter sebagaimana rumus:
Kalorimeter bom (kalorimetri volum konstan)
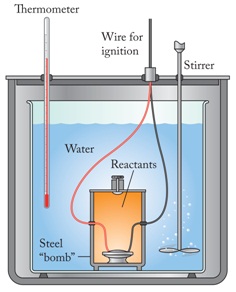
Kalorimeter bom
(Sumber: Gilbert, Thomas N. et al. 2012. Chemistry: The Science in Context (3rd edition). New York: W. W. Norton & Company, Inc.)
Pada kalorimeter bom berlaku rumus:
[V konstan]
Kalorimeter sederhana (kalorimetri tekanan konstan)
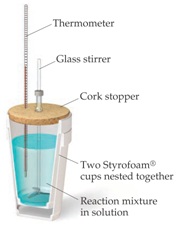
Termokimia: Kalorimeter sederhana
(Sumber: Petrucci, Ralph H. et al. 2011. General Chemistry: Principles and Modern Applications (10th edition). Toronto: Pearson Canada Inc.)
Pada kalorimeter sederhana berlaku rumus:
[V konstan]
Entalpi Pembentukan Standar dan Reaksi
Entalpi pembentukan standar, ΔHf°, didefinisikan sebagai perubahan entalpi dalam reaksi pembentukan 1 mol senyawa dari unsur-unsur penyusunnya pada keadaan standar (tekanan 1 atm, temperatur 298 K). Entalpi pembentukan standar dari unsur-unsur dalam bentuk paling stabil (seperti C (grafit), H2 (g), N2 (g), Ca (s)) didefinisikan sama dengan 0. Dari nilai-nilai entalpi pembentukan standar, dapat dihitung nilai entalpi reaksi standar, ΔHrx°, yaitu perubahan entalpi dalam reaksi pada keadaan standar.
Sebagai contoh, pada reaksi hipotetis berikut di mana a, b, c, dan d adalah koefisien stoikiometrik,
aA + bB → cC + dD
Hukum Hess
Hukum Hess menyatakan bahwa ketika reaktan terkonversi menjadi produk, nilai perubahan entalpi dari reaksi tetap sama, baik dengan satu langkah ataupun dengan sederetan langkah. Dengan kata lain, perubahan entalpi dari keseluruhan proses sama dengan jumlah total perubahan entalpi setiap langkah. Perhatikan contoh berikut.
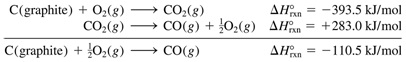
Dalam penerapan hukum Hess, kadangkala persamaan termokimia yang tersedia perlu dimanipulasi terlebih dahulu. Berikut aturan dalam memanipulasi persamaan termokimia:
- Ketika persamaan reaksi dibalik (reaktan menjadi produk, produk menjadi reaktan), tanda nilai ΔH juga harus dibalik (dari positif menjadi negatif, dan sebaliknya).
- Substansi yang dihilangkan dari kedua sisi persamaan reaksi harus dalam fase yang sama.
- Jika semua koefisien dari suatu persamaan reaksi dikali atau dibagi dengan faktor yang sama, maka nilai ΔH reaksitersebut juga harus dikali atau dibagi dengan faktor tersebut.
Pendekatan Energi Ikatan dan Entalpi Reaksi
Energi ikatan (entalpi ikatan), D, adalah energi yang dibutuhkan untuk memutus ikatan pada 1 mol molekul dalam fase gas. Entalpi reaksi dapat diestimasi dari total energi ikatan dari ikatan yang putus dikurangi total energi ikatan dari ikatan yang terbentuk.
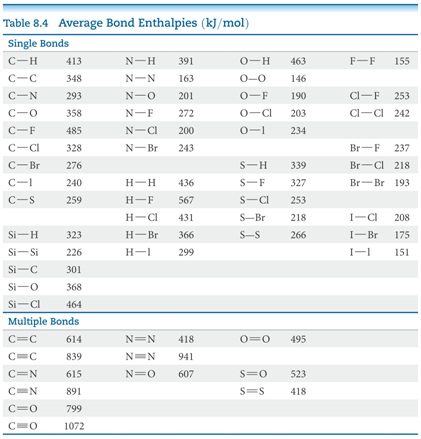
Tabel energi ikatan rata-rata
(Sumber: Brown, Theodore L. et al. 2015. Chemistry: The Central Science (13th edition). New Jersey: Pearson Education, Inc.)
Contoh soal
Estimasilah nilai pembakaran berikut dari data energi ikatan rata-rata pada tabel di atas.
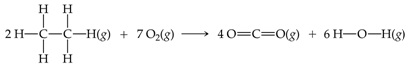
Jawab:
ΔH = ∑D(reaktan) − ∑D(produk)
= [12D(C−H) + 2D(C−C) + 7D(O=O)] –[8D(C=O) + 12D(O−H)]
= [12(413 kJ) + 2(348 kJ) + 7(495 kJ)] – [8(799 kJ) + 12(463 kJ)]
= 9117 kJ – 11948 kJ
ΔH = −2831 kJ
Termokimia – Referensi
– Brown, Theodore L. et al. 2015. Chemistry: The Central Science (13th edition). New Jersey: Pearson Education, Inc.
– Chang, Raymond. 2010. Chemistry (10th edition). New York: McGraw Hill
– Gilbert, Thomas N. et al. 2012. Chemistry: The Science in Context (3rd edition). New York: W. W. Norton & Company, Inc.
– Jespersen, Neil D., Brady, James E., & Hyslop, Allison. Chemistry: The Molecular Nature of Matter (6th edition). New Jersey: John Wiley & Sons, Inc.
– Petrucci, Ralph H. et al. 2011. General Chemistry: Principles and Modern Applications (10th edition). Toronto: Pearson Canada Inc.
– Purba, Michael. 2006. Kimia 2A untuk SMA Kelas XI. Jakarta: Erlangga.
– Silberberg, Martin S. 2009. Chemistry: The Molecular Nature of Matter and Change (5th edition). New York: McGraw Hill
– Stacy, Angelica M. 2015. Living by Chemistry (2nd edition). New York: W.H. Freeman and Company
Judul Artikel: Termokimia
Kontributor: Nirwan Susianto, S.Si.
Alumni Kimia UI
Materi StudioBelajar.com lainnya:

Leave a Comment