Benzena merupakan salah satu bahan kimia yang banyak digunakan dalam industri kimia, terutama sebagai prekursor dalam sintesis berbagai bahan kimia lainnya. Benzena tergolong senyawa hidrokarbon aromatik. Istilah “aromatik” ini diberikan karena pada saat pertama kali ditemukan banyak senyawa golongan ini yang memiliki aroma yang khas. Namun, kini istilah “aromatik” dikaitkan dengan struktur dan sifat-sifat khas tertentu, selain dari aromanya. Hal ini dikarenakan belakangan diketahui ada pula senyawa-senyawa aromatik yang tidak berbau.
Struktur Benzena
Benzena memiliki rumus kimia C6H6. Perbandingan jumlah atom C dan H-nya menunjukkan bahwa benzena sangat tidak jenuh. Pada mulanya, para ahli mengusulkan bahwa benzena memiliki struktur alifatik dengan adanya ikatan rangkap dua ataupun tiga. Namun, faktanya benzena tidak memperlihatkan sifat ketidakjenuhan dari struktur demikian. Hasil eksperimen menunjukkan sifat-sifat benzena seperti:
- Benzena ternyata sangat stabil (tidak reaktif).
Benzena tidak bereaksi dengan Br2, kecuali dengan bantuan katalis. Hal ini tidak sesuai dengan sifat ketidakjenuhan alkena ataupun alkuna yang mudah diadisi oleh bromin.
- Monosubstitusi atom halogen (X) pada benzena hanya menghasilkan satu jenis senyawa, yaitu C6H5Hal ini menunjukkan bahwa tidak terdapat keisomeran geometri sebagaimana pada alkena.
Pada tahun 1865, August Kekulé mengajukan struktur benzena sebagai suatu cincin yang terdiri dari 6 atom C dengan ikatan tunggal dan ikatan rangkap dua yang berselang-seling. Namun demikian, struktur ini kembali tidak dapat menjelaskan sifat-sifat benzena seperti:
- Benzena meskipun memiliki ikatan rangkap dua cenderung mengalami reaksi substitusi, bukan reaksi adisi seperti alkena umumnya.
- Berdasarkan pengukuran dengan difraksi sinar-X, benzena hanya memiliki satu panjang ikatan antar atom C yaitu 0,139 nm, yang menunjukkan bahwa semua ikatan dalam benzena sama/setara.
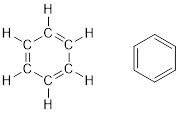
Model struktur benzena menurut Kekulé.
Berdasarkan fakta demikian, pada tahun 1931, Linus Pauling kemudian merumuskan struktur benzena sebagai struktur hibrida resonansi, yaitu struktur yang berada di antara dua struktur Kekulé. Struktur ini membentuk sistem delokalisasi elektron yang menstabilkan struktur.
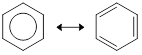
Struktur resonansi dari benzena menurut Linus Pauling.
Tanda ↔ menunjukkan beresonansi, bukan setimbang.
Struktur hibrida resonansi benzena dengan lingkaran dalam cincin menunjukkan adanya delokalisasi elektron.
Tata Nama Turunan Benzena
Senyawa turunan benzena dapat dianggap berasal dari benzena yang di mana satu atau lebih atom H-nya diganti dengan substituen lain berupa atom seperti −Br ataupun gugus atom seperti −COOH. Berikut aturan penamaan untuk senyawa-senyawa turunan benzena.
- Jika satu atom H pada benzena diganti satu substituen seperti −Cl, −CH3, −NO2, −NH2, −OH, −CHO, dan lain-lain, maka struktur dan penamaannya seperti berikut.
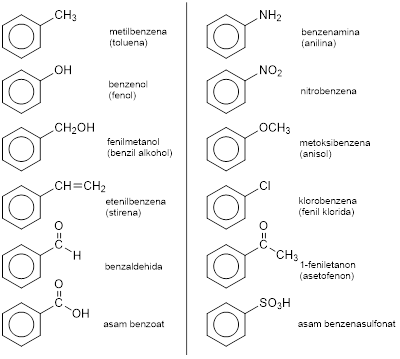
- Jika terdapat lebih dari satu substituen, maka diberi penomoran searah atau berlawanan arah jarum jam agar substituen-substituen mendapat nomor serendah mungkin. Untuk substituen-substituen sejenis, digunakan awalan di-, tri-, tetra-, penta-, dan heksa-. Urutan prioritas penomoran untuk beberapa substituen umum yaitu sebagai berikut.
−COOH, −SO3H, −COOR, −CN, −CHO, −CO, −OH, −NH2, −OR, −R, −X (F, Cl, Br, I), −NO2
Jika terdapat dua substituen, selain dengan penomoran, juga dapat digunakan awalan o-(orto) untuk posisi atom karbon nomor 1 dan 2, m-(meta) untuk posisi 1 dan 3, atau p-(para) untuk posisi 1 dan 4.
Contoh:
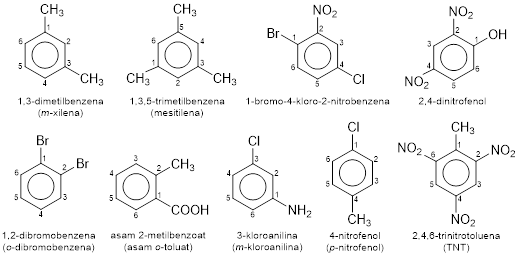
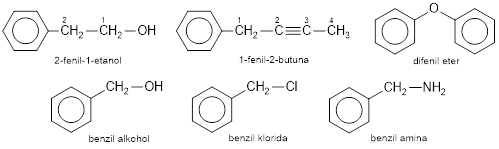
- Jika cincin benzena dianggap sebagai substituen, bukan sebagai induk, maka gugus benzena yang kehilangan satu atom H (C6H5−) disebut gugus fenil. Sedangkan, gugus metilbenzena (toluena) yang kehilangan satu atom H (C6H5CH2−) disebut gugus benzil.
Contoh:
Sifat-sifat Benzena
Benzena termasuk senyawa beracun dan bersifat karsinogenik (dapat menyebabkan kanker). Benzena berwujud cair pada suhu ruang, tidak berwarna, dan mudah menguap. Titik lelehnya 6°C dan titik didihnya 80°C. Strukturnya yang simetris dan planar menyebabkan susunannya sebagai kristal lebih rapat dan akibatnya titik lelehnya lebih tinggi dibandingkan heksana (−95°C). Seperti senyawa hidrokarbon lainnya, benzena juga bersifat nonpolar. Oleh karena itu, benzena larut dalam pelarut kurang polar atau nonpolar seperti eter dan tetraklorometana, namun tidak larut dalam pelarut polar seperti air.
Benzena cenderung tidak begitu reaktif, namun mudah terbakar. Akibat adanya sistem delokalisasi elektron yang menstabilkan benzena, benzena cenderung mudah mengalami reaksi substitusi dibanding reaksi adisi. Reaksi substitusi pada benzena melibatkan serangan pereaksi bermuatan positif parsial ataupun utuh yang suka elektron (elektrofil) pada cincin benzena. Oleh karena itu, reaksi substitusi pada benzena sering disebut sebagai reaksi substitusi elektrofilik. Reaksi-reaksi substitusi pada benzena, antara lain:
- Halogenasi
Benzena bereaksi dengan halogen seperti Cl2 dan Br2 dengan bantuan katalis besi(III) halida (FeCl3 atau FeBr3) membentuk senyawa halobenzena.
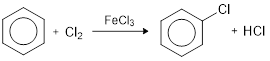
- Nitrasi
Benzena bereaksi dengan asam nitrat pekat dengan katalis asam sulfat pekat membentuk nitrobenzena.
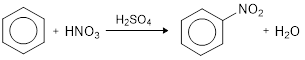
- Sulfonasi
Benzena bereaksi dengan SO3 dalam asam sulfat pekat bila dipanaskan membentuk asam benzenasulfonat.
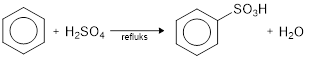
- Alkilasi Friedel-Crafts
Benzena bereaksi dengan alkil halida dengan bantuan katalis aluminium klorida (AlCl3) membentuk alkilbenzena.
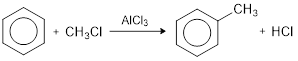
Kegunaan Benzena dan Turunannya
- Benzena digunakan sebagai pelarut dan juga bahan dasar sintesis berbagai senyawa turunan benzena seperti stirena, dan lain-lain.
- Fenol bersifat asam lemah dan dapat digunakan sebagai bahan dasar pembuatan plastik dan obat-obatan. Fenol juga dapat digunakan sebagai antiseptik dan disinfektan oleh karena sifatnya yang dapat mendenaturasi protein.
- Toluena digunakan sebagai pelarut dan bahan baku pembuatan asam benzoat, bahan peledak TNT, dan lain-lain.
- Asam benzoat digunakan sebagai bahan pengawet makanan dan minuman.
- Anilina digunakan untuk membuat zat-zat pewarna diazo.
- Asam salisilat digunakan untuk membuat aspirin, perasa, minyak wangi, bedak, salep anti jamur, dan sampo.
Contoh Soal Benzena dan Pembahasan
Contoh Soal 1
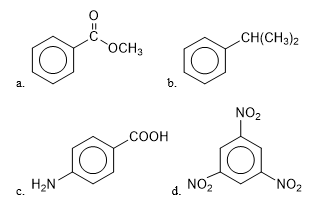
Tulislah nama dari senyawa-senyawa turunan benzena berikut.
Jawab:
a. metil benzoat
b. isopropil benzena
c. asam p-aminobenzoat (asam 4-aminobenzoat)
d. 1,3,5-trinitrobenzena
Contoh Soal 2
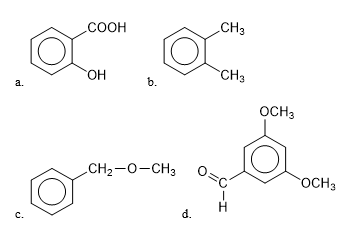
Gambarkan struktur dari senyawa-senyawa turunan benzena berikut.
a. asam salisilat (asam 2-hidroksibenzoat)
b. o-xilena
c. benzil metil eter
d. 3,5-dimetoksibenzaldehid
Jawab:
Referensi
Brown, Theodore L. et al. 2015. Chemistry: The Central Science (13th edition). New Jersey: Pearson Education, Inc.
Johari, J.M.C. & Rachmawati, M. 2008. Kimia SMA dan MA untuk Kelas XII Jilid 3. Jakarta: Esis
Okuyama, Tadashi & Maskill, Howard. 2014. Organic Chemistry: a mechanistic approach. Oxford: Oxford University Press
Purba, Michael. 2007. Kimia 3B untuk SMA Kelas XII. Jakarta: Erlangga
Wade, L.G. & Simek, J.W. 2016. Organic Chemistry (9th edition). Harlow: Pearson Education Limited
Kontributor: Nirwan Susianto, S.Si.
Alumni Kimia FMIPA UI
Materi StudioBelajar.com lainnya:

Leave a Comment